先天性免疫反應是機體防御外來病原微生物感染的第一道防線,這種快速非特異性的反應依賴于模式識別受體對病原相關分子模式的識別與結合。核苷酸寡聚化結構域樣受體(Nucleotide oligomerization domain-like receptors, NLRs)家族成員NOD1是經典的抗細菌相關的胞內模式識別受體,盡管已有研究顯示脊椎動物的NOD1參與機體抗病毒免疫反應,但其具體的作用機制仍不清楚。
中國科學院水生生物研究所研究員昌鳴先團隊發現,在正常的生理條件下,NOD1基因的敲除顯著損害促炎性細胞因子以及視黃酸誘導基因-I樣受體(Retinoic acid inducible gene I like receptors, RLRs)所介導的抗病毒信號通路中關鍵靶基因的轉錄,這表明NOD1缺陷魚已經有一個受損的免疫系統。在病毒感染的情況下,NOD1基因的敲除將影響病毒復制以及幼魚存活。進一步研究發現,NOD1可以作為SVCV(ssRNA 病毒)的受體,識別并結合SVCV;NOD1不僅能增強MDA5a與poly I:C(dsRNA)的結合,而且能通過靶向MDA5剪接異構體和TRAF3,正調控MDA5a-MAVS和TRAF3-MAVS復合體的形成,從而誘導干擾素和干擾素刺激基因(ISGs)的產生。此外,該研究也顯示NOD1增強MDA5與dsRNA結合、正調控MDA5-MAVS復合體形成的作用保守存在于哺乳動物中。有趣的是,魚類MDA5剪接異構體MDA5a與MDA5b對NOD1的調控呈現截然相反的方式,MDA5a能夠增強NOD1蛋白的表達,但是MDA5b卻通過泛素-蛋白酶體途徑降解NOD1蛋白。由于哺乳動物MDA5不存在選擇性剪接,因此MDA5短型的剪接異構體對NOD1蛋白的降解作用特異存在于硬骨魚類中。
該研究首次揭示了魚類NOD1和MDA5剪接異構體的相互作用調控先天免疫反應的作用機制。相關研究結果于3月13日在線發表于免疫學經典期刊The Journal of Immunology,水生所博士生武小曼和助理研究員張杰為該文的共同第一作者,昌鳴先為通訊作者。該研究得到中科院A類戰略性先導科技專項(XDA24010308)、國家自然科學基金面上項目(31672687和31873046)、湖北省自然科學基金創新群體項目(2018CFA011)資助。
文章鏈接https://www.jimmunol.org/content/early/2020/03/12/jimmunol.1900667
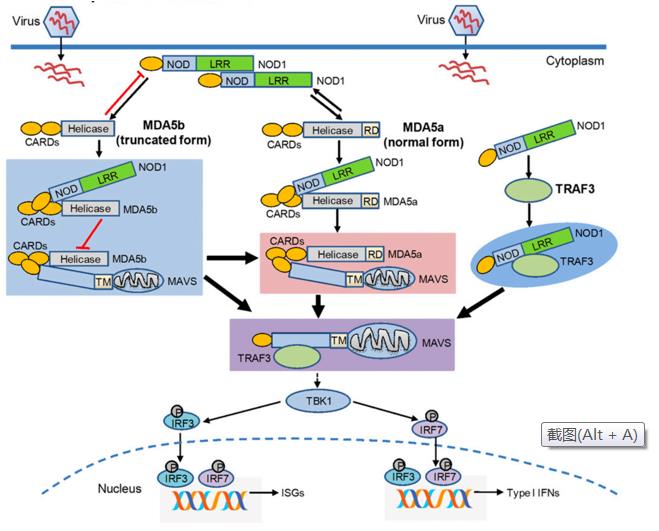
魚類NOD1調控先天免疫反應的作用模型圖